| Cachexia | |
|---|---|
| Andre navn | Wasting syndrom |
 |
|
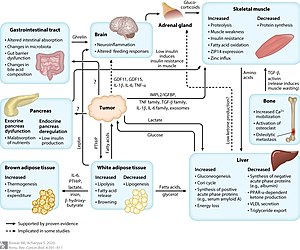
| Prosesser og mekanismer relatert til kreftassosiert kakeksi | |
| Spesialitet | Onkologi, indremedisin, fysisk medisin og rehabilitering |
| Symptomer | plutselig vekttap, endrede spisesignaler |
| Prognose | svært dårlig |
| Frekvens | 1% |
| Dødsfall | 1,5 til 2 millioner mennesker i året |
Cachexia er et komplekst syndrom assosiert med en underliggende sykdom som forårsaker pågående muskeltap som ikke er helt reversert med ernæringstilskudd. En rekke sykdommer kan forårsake kakeksi, ofte kreft, hjertesvikt, kronisk obstruktiv lungesykdom, kronisk nyresykdom og AIDS. Systemisk betennelse fra disse tilstandene kan forårsake skadelige endringer i metabolisme og kroppssammensetning. I motsetning til vekttap fra utilstrekkelig kaloriinntak, forårsaker kakeksi hovedsakelig muskeltap i stedet for fett tap. Diagnostisering av kakeksi kan være vanskelig på grunn av mangel på veletablerte diagnostiske kriterier. Kakeksi kan forbedres ved behandling av den underliggende sykdommen, men andre behandlingsmetoder har begrenset fordel. Kakeksi er assosiert med økt dødelighet og dårlig livskvalitet.
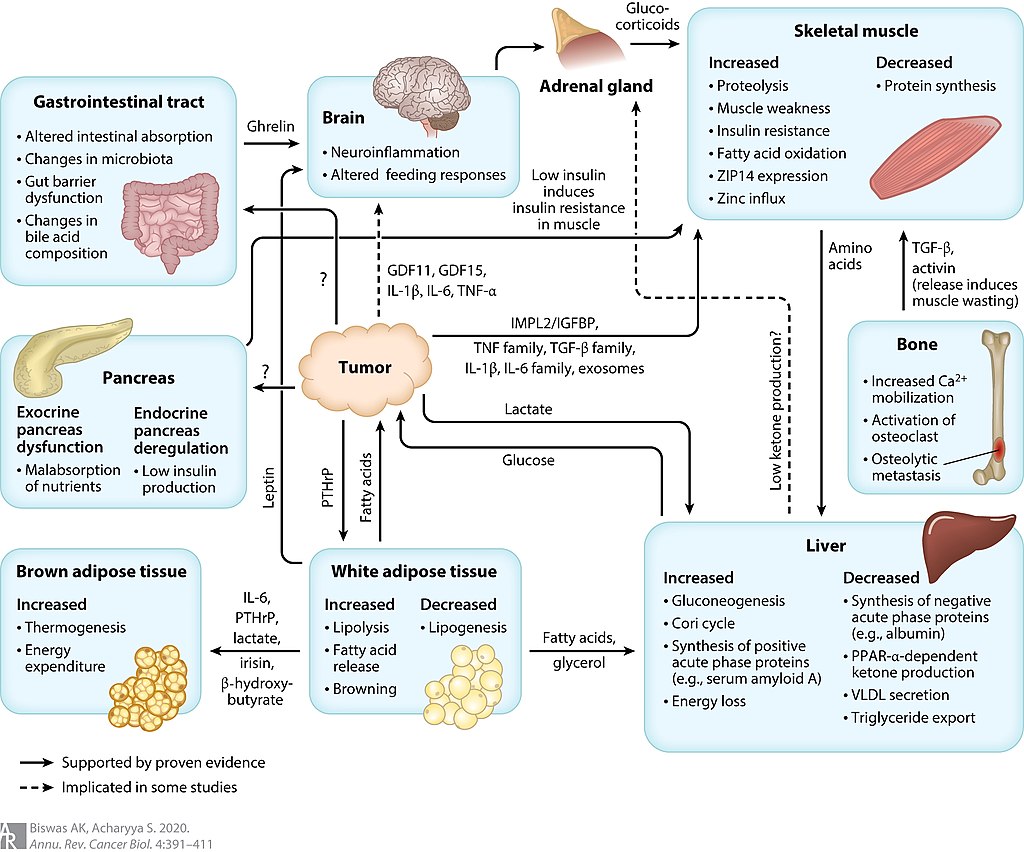
Hva forårsaker kakeksi?
Kakeksi kan være forårsaket av forskjellige medisinske tilstander, men er ofte forbundet med sluttkreft, kjent som kreftkakeksi. Cirka 50% av alle kreftpasienter lider av kakeksi. De med øvre gastrointestinale kreft og bukspyttkjertelkreft har den høyeste frekvensen for å utvikle et kakeksisk symptom. Prevalensen av kakeksi øker i mer avanserte stadier og anslås å påvirke 80% av terminal kreftpasienter.
Kongestiv hjertesvikt, AIDS, kronisk obstruktiv lungesykdom og kronisk nyresykdom er andre tilstander som ofte forårsaker kakeksi. Kakeksi kan også være et resultat av avanserte stadier av cystisk fibrose, multippel sklerose, motorisk neuronsykdom, Parkinsons sykdom, demens, tuberkulose, multippel systematrofi, kvikksølvforgiftning, Crohns sykdom, revmatoid artritt og cøliaki, så vel som andre systemiske sykdommer.
Mekanisme for kakeksi
Den nøyaktige mekanismen der disse sykdommene forårsaker kakeksi er dårlig forstått, og er sannsynligvis multifaktoriell med flere sykdomsveier involvert. Inflammatoriske cytokiner ser ut til å spille en sentral rolle, inkludert TNF (som også er kalt «kakeksin» eller «kakektin»), interferon gamma og interleukin 6. TNF har vist seg å ha en direkte katabolsk effekt på skjelettmuskulatur og fettvev gjennom ubiquitinproteasomet. sti. Denne mekanismen involverer dannelsen av reaktive oksygenarter som fører til oppregulering av transkripsjonsfaktoren NF-KB. NF-KB er en kjent regulator av genene som koder for cytokiner og cytokinreseptorer. Den økte produksjonen av cytokiner induserer proteolyse og nedbrytning av myofibrillære proteiner. Systemisk betennelse forårsaker også redusert proteinsyntese gjennom inhibering av Akt / mTOR-banen.
Selv om mange forskjellige vev og celletyper kan være ansvarlige for økningen i sirkulerende cytokiner, tyder bevis på at svulster i seg selv er en viktig kilde til faktorer som kan fremme kakeksi i kreft. Tumor-avledede molekyler som lipidmobiliserende faktor, proteolyse-induserende faktor og mitokondrie-frakoblingsproteiner kan indusere proteinnedbrytning og bidra til kakeksi. Ukontrollert betennelse i kakeksi kan føre til forhøyet hvilestoffskifte, noe som ytterligere øker kravene til protein og energikilder.
Det er også bevis for endring i fôringskontrollløkker i kakeksi. Høye nivåer av leptin, et hormon utskilt av adipocytter, blokkerer frigjøringen av nevropeptid Y, som er det mest potente fôringsstimulerende peptidet i det hypotalamus orexigenic nettverket, noe som fører til redusert energiinntak til tross for den høye metabolske etterspørselen etter næringsstoffer.
Diagnose av kakeksi
Diagnostiske retningslinjer og kriterier er bare nylig foreslått til tross for utbredelsen av kakeksi og varierende kriterier. De viktigste egenskapene til kakeksi inkluderer progressiv utarmning av muskel- og fettmasse, redusert matinntak, unormal metabolisme av karbohydrat, protein og fett, redusert livskvalitet , og økt fysisk funksjonshemning.
Historisk ble kroppsvektendringer brukt som de primære beregningene av kakeksi, inkludert lav kroppsmasseindeks og ufrivillig vekttap på mer enn 10%. Å bruke vekt alene er begrenset av tilstedeværelsen av ødem, svulstmasse og den høye prevalensen av fedme i befolkningen generelt. Vektbaserte kriterier tar ikke hensyn til endringer i kroppssammensetning, spesielt tap av mager kroppsmasse.
I forsøket på å inkludere en bredere evaluering av belastningen ved kakeksi, er diagnostiske kriterier foreslått ved bruk av vurderinger av laboratoriemetrikker og symptomer i tillegg til vekt. Kriteriene inkluderte vekttap på minst 5% i 12 måneder eller lav kroppsmasseindeks (mindre enn 22 kg / m2) med minst tre av følgende funksjoner: redusert muskelstyrke, utmattelse, anoreksi, lav fettfri masseindeks eller unormal biokjemi (økte betennelsesmarkører, anemi, lavt serumalbumin). Hos kreftpasienter diagnostiseres kakeksi ved utilsiktet vekttap på mer enn 5%. For kreftpasienter med en kroppsmasseindeks på mindre enn 20 kg / m2, diagnostiseres kakeksi etter utilsiktet vekttap på mer enn 2%. I tillegg kan det diagnostiseres gjennom sarkopeni, eller tap av skjelettmuskelmasse.
Laboratoriemarkører brukes til evaluering av personer med kakeksi, inkludert albumin, prealbumin, C-reaktivt protein eller hemoglobin. Imidlertid er laboratorieberegninger og grenseverdier ikke standardisert på tvers av forskjellige diagnostiske kriterier. Akutte fase-reaktanter (IL-6, IL-1b, tumornekrosefaktor-a, IL-8, interferon-g) måles noen ganger, men korrelerer dårlig med utfallet. Det er ingen biomarkører for å identifisere mennesker med kreft som kan utvikle kakeksi.
I arbeidet med å klassifisere alvorlighetsgraden av kakeksi, har flere poengsystemer blitt foreslått, inkludert Cachexia Staging Score (CSS) og Cachexia Score (CASCO). CSS tar hensyn til vekttap, subjektiv rapportering av muskelfunksjon, ytelsesstatus, tap av appetitt og laboratorieendringer for å kategorisere pasienter i ikke-kakeksi, pre-kakeksi, kakeksi og ildfast kakeksi. Cachexia SCOre (CASCO) er en annen validert poengsum som inkluderer evaluering av kroppsvektstap og sammensetning, betennelse, metabolske forstyrrelser, immunsuppresjon, fysisk ytelse, anoreksi og livskvalitet.
Evaluering av endringer i kroppssammensetning er begrenset av vanskeligheten med å måle muskelmasse og helse på en ikke-invasiv og kostnadseffektiv måte. Bildebehandling med kvantifisering av muskelmasse har blitt undersøkt, inkludert bioelektrisk impedansanalyse, computertomografi, dobbel-energi røntgenabsorptiometri (DEXA) og magnetisk resonansavbildning, men brukes ikke mye.
Definisjon av kakeksi
Identifisering, behandling og forskning av kakeksi har historisk vært begrenset av mangelen på en allment akseptert definisjon av kakeksi. I 2011 vedtok en internasjonal konsensusgruppe en definisjon av kakeksi som “et multifaktorielt syndrom definert av et pågående tap av skjelettmuskelmasse (med eller uten tap av fettmasse) som kan være delvis, men ikke helt reversert av konvensjonell ernæringsstøtte”.
Kakeksi skiller seg fra vekttap på grunn av underernæring fra malabsorpsjon, anorexia nervosa eller anoreksi på grunn av alvorlig depressiv lidelse. Vekttap fra utilstrekkelig kaloriinntak forårsaker vanligvis fett tap før muskeltap, mens kakeksi forårsaker hovedsakelig muskelsvinn. Kakeksi skiller seg også fra sarkopeni eller aldersrelatert muskeltap, selv om de ofte eksisterer samtidig.
Behandling av kakeksi
Behandlingen av kakeksi avhenger av den underliggende årsaken, den generelle prognosen og behovene til den berørte personen. Den mest effektive tilnærmingen til kakeksi er behandling av den underliggende sykdomsprosessen. Et eksempel er reduksjon i kakeksi fra AIDS ved høyt aktiv antiretroviral terapi. Dette er imidlertid ofte ikke mulig eller kanskje utilstrekkelig til å reversere kakeksiasyndrom i andre sykdommer. Tilnærminger for å redusere muskeltap inkluderer trening, ernæringsterapi og medisiner.
Trening
Terapi som inkluderer regelmessig fysisk trening anbefales for behandling av kakeksi på grunn av de positive effektene av trening på skjelettmuskulaturen. Personer med kakeksi rapporterer vanligvis lave nivåer av fysisk aktivitet, og få deltar i en treningsrutine på grunn av lav motivasjon for å trene og en tro på at trening kan forverre symptomene eller forårsake skade.
Medisiner
Appetittstimulerende medisiner brukes til å behandle kakeksi for å øke matinntaket, men er ikke effektive for å stoppe muskelsvinn og kan ha skadelige bivirkninger. Appetittstimulerende midler inkluderer glukokortikoider, cannabinoider eller progestiner som megestrolacetat. Anti-emetika som 5-HT3 antagonister brukes også ofte i kreftkakeksi hvis kvalme er et fremtredende symptom.
Anabole-androgene steroider som oksandrolon kan være gunstige i kakeksi, men deres bruk anbefales i maksimalt to uker siden en lengre behandlingsvarighet øker bivirkningene. Mens foreløpige studier har antydet at talidamid kan være nyttig, fant en Cochrane-gjennomgang ingen bevis for å ta en informert beslutning om bruk av dette legemidlet hos kreftpasienter med kakeksi.
Ernæring
Den økte metabolske hastigheten og appetittundertrykkelsen som er vanlig i kakeksi, kan føre til muskeltap. Studier med kaloritett proteintilskudd har antydet at minst vektstabilisering kan oppnås, selv om forbedringer i magert kroppsmasse ikke har blitt observert i disse studiene.
Kosttilskudd
Administrering av eksogene aminosyrer har blitt undersøkt for å tjene som et proteinbesparende metabolsk drivstoff ved å tilveiebringe substrater for både muskelmetabolisme og glukoneogenese. De forgrenede aminosyrene leucin og valin kan ha potensiale i å hemme overekspresjon av proteinnedbrytningsveier. Aminosyren glutamin har blitt brukt som en komponent av oral tilskudd for å reversere kakeksi hos personer med avansert kreft eller HIV / AIDS.
β-hydroksy β-metylbutyrat (HMB) er en metabolitt av leucin som fungerer som et signalmolekyl for å stimulere proteinsyntese. Studier viste positive resultater for kronisk lungesykdom, hoftebrudd og ved AIDS-relatert og kreftrelatert kakeksi. Imidlertid brukte mange av disse kliniske studiene HMB som en komponent i kombinasjonsbehandling med glutamin, arginin, leucin, høyere diettprotein og / eller vitaminer, noe som begrenser vurderingen av effekten av HMB alene.
Epidemiologi
Nøyaktige epidemiologiske data om utbredelsen av kakeksi mangler på grunn av endrede diagnostiske kriterier og underidentifisering av personer med sykdommen. Det anslås at kakeksi fra en hvilken som helst sykdom anslås å påvirke mer enn 5 millioner mennesker i USA. Forekomsten av kakeksi vokser og anslås til omtrent 1% av befolkningen. Forekomsten er lavere i Asia, men på grunn av den større befolkningen, representerer den en lignende byrde. Cachexia er også et betydelig problem i Sør-Amerika og Afrika.
De hyppigste årsakene til kakeksi i USA etter populasjonsutbredelse er: 1) KOLS, 2) hjertesvikt, 3) kreftkakeksi, 4) kronisk nyresykdom. Forekomsten av kakeksi varierer fra 15–60% blant mennesker med kreft, og øker til anslagsvis 80% i terminal kreft. Dette brede spekteret tilskrives forskjeller i definisjon av kakeksi, variasjon i kreftpopulasjoner og tidspunkt for diagnose. Selv om utbredelsen av kakeksi blant personer med KOLS eller hjertesvikt er lavere (estimert 5% til 20%), øker det store antallet mennesker med disse tilstandene den totale kakeksi byrden dramatisk.
Cachexia bidrar til betydelig tap av funksjon og helsetjenester. Anslag ved bruk av National Inpatient Sample i USA antyder at kakeksi utgjorde 177 640 sykehusopphold i 2016. Kakeksi regnes som den umiddelbare dødsårsaken til mange mennesker med kreft, anslått mellom 22-40%.
.


Discussion about this post